Een wereldleider gespecialiseerd in de distributie van biosimilars
Een biologisch gelijkwaardig geneesmiddel, een biosimilar, is zodanig ontwikkeld dat het biologisch identiek is aan een eerder goedgekeurd biologisch geneesmiddel (het referentieproduct) met dezelfde werkzame stoffen, waarna bewezen is dat het inderdaad biologisch gelijkwaardig is. De biosimilar, bekend om zijn goede kwaliteit en betaalbaarheid, is een innovatief medicijn geworden voor patiënten met verschillende ziekten over de hele wereld, waaronder Europa en de Verenigde Staten.
-
De eerste biosimilar rituximab goedgekeurd
door de FDA - Celltrion Group betrad in 2018 de grootste markt ter wereld met het verkrijgen van de goedkeuring van de Amerikaanse Food and Drug Administration (FDA) voor de biosimilar rituximab. De biosimilars voor oncologie van Celltrion Healthcare worden in Europa en andere delen van de wereld op grote schaal voorgeschreven en krijgen positieve beoordelingen van patiënten, artsen en andere relevante instanties. Daarom wordt verwacht dat deze biosimilars voor oncologie ook goed zullen worden ontvangen in de Verenigde Staten.
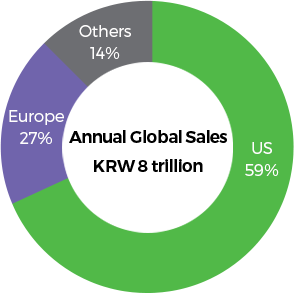 Source : IQVIA 2018
Source : IQVIA 2018
- De pionier in mAb biosimilars voor oncologie
- Celltrion Healthcare heeft haar competenties getoond door de snelle groei op het gebied van behandelingen voor kankerbestrijding. Celltrion Healthcare lanceerde haar eerste biosimilar voor oncologie in 2017 in Europa, en kende een snelle groei binnen een jaar na de lancering. In het kielzog van het succes van de bestaande producten wordt ook de andere biosimilar voor oncologie, die in 2018 in Europa werd gelanceerd, op grote schaal voorgeschreven.